L’énergie représente l’un des paramètres les plus fondamentaux de la physiologie et, en ce qui concerne l’homéostasie énergétique, les mitochondries sont des organites cruciaux car elles fournissent la majorité de cette énergie sous la forme d’adénosine triphosphate (ATP). Pour produire cet ATP, les mitochondries utilisent différentes sources d’énergie qui sont métabolisées à travers un réseau complexe. Parallèlement à cette production d’énergie, le métabolisme mitochondrial génère une variété de métabolites essentiels et contrôle également l’homéostasie des ions et des molécules de signalisation tels que le calcium, les espèces réactives de l’oxygène ou les neurotransmetteurs. Par conséquent, les mitochondries sont des structures centrales pour le métabolisme cellulaire, mais aussi pour la santé globale des cellules.
Les fonctions métaboliques des mitochondries se déroulent principalement dans les compartiments internes des mitochondries : la matrice mitochondriale et la membrane interne. Ces compartiments sont entourés d’une seconde membrane, la membrane mitochondriale externe. Malgré cette localisation intégrée, ces activités métaboliques doivent être constamment et finement orchestrées pour s’adapter à la disponibilité des substrats et aux besoins physiologiques.
Les données protéomiques de la littérature ainsi que nos propres études protéomiques révèlent que de nombreuses protéines métaboliques mitochondriales sont ubiquitinylées. Cependant, leur implication dans la régulation du métabolisme mitochondrial est encore inconnue. Le but de notre projet est de disséquer le rôle joué par le système ubiquitine-protéasome SUP concernant le métabolisme énergétique mitochondrial.
Pour atteindre ce but, nous avons défini trois objectifs spécifiques :
- Caractériser l’ubiquitome mitochondrial et le renouvellement des protéines intra-mitochondriales dépendant du SUP.
- Identifier et caractériser les E3 ubiquitine ligases mitochondriales.
- Définir les conséquences physiologiques de la régulation des protéines intramitochondriales en fonction du SUP.
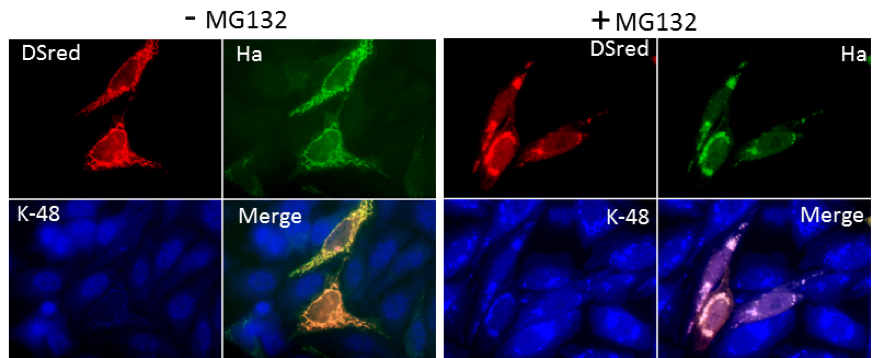
Accumulation de la protéine K48 ubiquitinée dans les mitochondries lors de l’inhibition du protéasome
Identification de l’interactome mitochondrial E3s par proteomique
Membres contributeurs
Giovanni Bénard [Directeur de Recherche CNRS, chercheur principal]
Victor Gindensperger [Ingénieur de Recherche]
Claude Lalou [Ingénieur d’étude Hors Classe]
Agata Ars [Technicienne]
Collaborations nationales et internationales :
Patryk Ngondo [Institut de Biologie Moléculaire des Plantes, Strasbourg, France]
Rajesh Singh [University of Baroda, India]
Timothy Shutt [University of Calgary, Canada]
Jean-William Dupuy [Proteomics Facility, University of Bordeaux, France]
METATOUL [INSA, INRAe, Toulouse]
Sélection de publications :
Lavie J, Lalou C, Mahfouf W, Dupuy JW, Lacaule A, Cywinska AA, Lacombe D, Duchêne AM, Raymond AA, Rezvani HR, Ngondo RP, Bénard G. The E3 ubiquitin ligase FBXL6 controls the quality of newly synthesized mitochondrial ribosomal proteins. Cell Rep. 2023 Jun 27;42(6):112579. Epub 2023 Jun 1. DOI: 10.1016/j.celrep.2023.112579
Lavie J, De Belvalet H, Sonon S, Ion AM, Dumon E, Melser S, Lacombe D, Dupuy JW, Lalou C, Bénard G. Ubiquitin-Dependent Degradation of Mitochondrial Proteins Regulates Energy Metabolism. Cell Report. 2018.
Hebert-Chatelain E, Desprez T, Serrat R, Bellocchio L, Soria-Gomez E, Busquets-Garcia A, Pagano Zottola AC, Delamarre A, Cannich A, Vincent P, Varilh M, Robin LM, Terral G, García-Fernández MD, Colavita M, Mazier W, Drago F, Puente N, Reguero L, Elezgarai I, Dupuy JW, Cota D, Lopez-Rodriguez ML, Barreda-Gómez G, Massa F, Grandes P, Bénard G*, Marsicano G*. A cannabinoid link between mitochondria and memory. Nature. 2016. [*Sharing senior authorship]
Lavie J, Serrat R, Bellance N, Courtand G, Dupuy JW, Tesson C, Coupry I, Brice A, Lacombe D, Durr A, Stevanin G, Darios F, Rossignol R, Goizet C, Bénard G. Mitochondrial morphology and cellular distribution are altered in SPG31 patients and are linked to DRP1 hyperphosphorylation. Hum. Mol. Genet. 2017.
Tomar D, Prajapati P, Lavie J, Singh K, Lakshmi S, Bhatelia K, Roy M, Singh R, Singh R*, Bénard G*. TRIM4; a novel mitochondrial interacting RING E3 ligase, sensitizes the cells to hydrogen peroxide (H2O2) induced cell death. Free Radic Biol Med. 2015. [*Sharing senior authorship]
Melser S, Hebert Chatelain E, Lavie J, Mahfouf W, Jose C, Obre E, Goorden S, Priaul M, Elgersma Y, Rezvan H, Rossignol R, Bénard G. Rheb regulates mitophagy induced by mitochondrial energetic status. Cell Metabolism. 2013.