Modulation bioénergétique mitochondriale (science fondamentale et découverte de médicaments)
Il est nécessaire de découvrir des médicaments capables de stimuler la fonction mitochondriale afin de remédier aux déficiences bioénergétiques d’un grand nombre de maladies rares. Aucun médicament capable d’activer ou de réparer la fonction mitochondriale n’est disponible en clinique à l’exception du bézafibrate, du resvératrol ou de l’ibédénone, qui ont montré une efficacité limitée chez un petit nombre de patients. Le projet vise à découvrir de nouvelles cibles actionnables (médicamenteuses) impliquées dans la régulation de la fonction mitochondriale et le contrôle de la qualité, et à développer, évaluer et breveter des médicaments nouveaux ou réorientés pour la thérapie bioénergétique. Une grande variété de modèles expérimentaux, allant des cellules cancéreuses aux myoblastes primaires humains ou aux cellules souches embryonnaires murines, est utilisée pour étudier la régulation moléculaire de la bioénergétique mitochondriale. Nous avons également développé et financé une plateforme bioénergétique organisée comme une société de services spin-out pour offrir des services à l’industrie pharmaceutique et effectuer un criblage innovant de médicaments pour la découverte de candidats bioénergétiquement actifs (www.cellomet.com). Les composés principaux sont ensuite testés dans des modèles cellulaires de maladies rares en collaboration avec les chercheurs cliniques du MRGM. Le projet MITOMODUL étudie également la toxicité mitochondriale des médicaments.
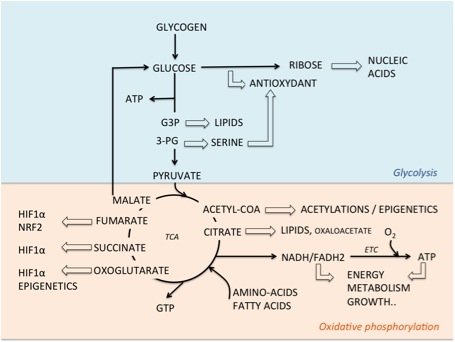
Les voies biochimiques du métabolisme énergétique jouent également un rôle central dans le contrôle de l’anabolisme, de l’expression des gènes et de l’épigénétique. Le décryptage des acteurs moléculaires impliqués dans cette interaction pourrait révéler des cibles moléculaires exploitables et intéressantes pour le développement de thérapies innovantes.
Membres contributeurs
Marija VLASKI (CR EFS)
Philippe BRUNET DE LA GRANGE (DR EFS)
Publications et brevets du projet
Targeting the mitochondrial trifunctional protein in oxidative lung carcinomas. [In revision].
EIF3F cooperates with STAT3 to regulate metastasis in human lung adenocarcinoma. [In revision].
3rd Prize (pitch). Meet2win_Oncology Business Convention [May 11th and 12th; Bordeaux]
PML-Regulated Mitochondrial Metabolism Enhances Chemosensitivity in Human Ovarian Cancers. Cell Metab. 2018 Sep 17.[Collaboration].
Redox mechanism of levobupivacaine cytostatic effect on human prostate cancer cells. Redox Biol. 2018 Sep. 18:33-42.
Energy Metabolism Rewiring Precedes UVB-Induced Primary Skin Tumor Formation. Cell Rep. 2018 Jun 19. 23(12):3621-3634 [Collaboration]
Drug discovery strategies in the field of tumor energy metabolism: Limitations by metabolic flexibility and metabolic resistance to chemotherapy. Biochim Biophys Acta Bioenerg. 2017 Aug. 1858(8):674-685. [Review]
High glucose repatterns human podocyte energy metabolism during differentiation and diabetic nephropathy. FASEB J. 2017 Jan. 31(1):294-307. 14.
Enhanced OXPHOS, glutaminolysis and β-oxidation constitute the metastatic phenotype of melanoma cells. Biochem J. 2016 Mar 15. 473(6):703-15 [Collaboration]
Redox Homeostasis and Mitochondrial Dynamics. Cell Metab. 2015 Aug 4. 22(2):207-18. (Review)
EP17306858.6. Mitochondrial trifunctional protein (MTP) inhibitors for use in the treatment of high mitochondrial respiration (OX+) cancers.
Financement du projet
H2020 ITN Marie Curie project TRANSMIT : Translating the role of mitochondria in tumorigenesis
Inca N° 2017-040. Priorité Tabac 2017
Cellomet services